|
 Teorija Teorija
Daug cheminių reakcijų vyksta
tirpaluose. Svarbus tirpalo rodiklis – koncentracija. Tirpalą sudaro
tirpiklis ir tirpinys (ištirpusi medžiaga). Tirpiklis gali būti:
vanduo, etanolis, benzenas, tetrachlormetanas ir kitos medžiagos.
Tirpalo molinė koncentracija rodo,
kiek molių ištirpusios medžiagos (tirpinio) yra viename litre (l)
arba viename kūbiniame decimetre (dm 3) tirpalo.
Molinė koncentracija reiškiama
mol/l, dažnai būna užrašoma tiesiog M. Žymima raide c.
 Formulės
Formulės

 Uždavinių sprendimo pavyzdžiai Uždavinių sprendimo pavyzdžiai
Uždavinys
1
|
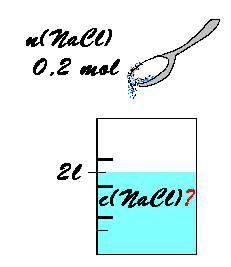
2
l tirpalo ištirpę
0,2 mol
valgomosios druskos. Raskite tirpalo molinę koncentraciją.
|
| Duota:v(NaCl) = 2
l n(NaCl) = 0,2 mol
Rasti:
c(NaCl)
Formulė:c(A) = n(A)
: v
Sprendimas:
c(NaCl) = 0,2 mol : 2
l
= 0,1 mol/l
Atsakymas: tirpalo koncentracija
0,1 mol/l
|
|
Uždavinys
2
Kiek molių cukraus yra 600
ml tirpalo,
kurio koncentracija 0,3 mol/l?
Duota:
v(t) = 600 ml = 0,6
l
c(C12H22O11) = 0,3 mol/l
Rasti:
n(C12H22O11)
Formulė:
n(A) = c(A) x v
Sprendimas:
n(C12H22O11)
= 0,3 mol/l
x 0,6
l = 0,18 mol
Atsakymas:
tirpale –
0,18 mol cukraus.
Uždavinys
3
Kiek litrų
0,15 mol/l koncentracijos tirpalo pagaminsime iš 0,5 mol medžiagos?
Duota:c(A)
= 0,15 mol/l
n(A) = 0,5 mol
Rasti:v
Formulė:v = n(A)
: c(A)
Sprendimas:
v = 0,5 mol : 0,15 mol/l
= 3,33
l
Atsakymas: tirpalo pagaminta 3,33
l.
Uždavinys
4
Turime
250 ml druskos rūgšties
tirpalo, kurio koncentracija 1,5 mol/l. Kokia masė HCl ištirpinta?
Duota:
v = 250 ml = 0,25
l
c(HCl) = 1,5 mol/l
Rasti:
n(HCl)
m(HCl)
Formulė:
n(A) = c(A) x v
m = n x M
Sprendimas:
- Randame
HCl molių skaičių:
n(HCl) = 1,5 mol/l x 0,25
l = 0,375 mol
- Randame
HCl molinę masę:
M(HCl) = 1 + 35,5 = 36,5 g/mol
- Randame
HCl masę:
m(HCl) = 0,375 mol x 36,5 g/mol = 13,6 g
Atsakymas: ištirpinta
13,6 g HCl.
Uždavinys
5
|
300 ml ištirpinta 14,6 g valgomosios
druskos. Raskite tirpalo molinę koncentraciją.
|
| Duota:
v(t) = 300 ml = 0,3
l
m(NaCl) = 14,6 g
Rasti:
w(NaCl)
c(NaCl)
Formulė:
n = m : M
c(A) = n(A)
: v
Sprendimas:
- Randame
NaCl molinę masę:
M(NaCl) = 23 + 35,5 = 58,5 g/mol
- Randame
NaCl molių skaičių:
n(NaCl) = 14,6 g : 58,5 g/mol = 0,25 mol
- Randame
molinė koncentraciją:
c(NaCl) = 0,25 mol : 0,3
l
= 0,833 mol/l
Atsakymas: koncentracija –
0,833 mol/l
|
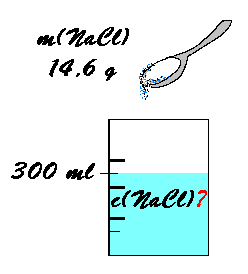 |
 Uždaviniai savarankiškam darbui Uždaviniai savarankiškam darbui
1.
600 dm
3 tirpalo yra ištirpę 0,3 mol gliukozės. Raskite tirpalo
koncentraciją.
Atsakymas
2. Laboratorijoje
paruošta 150 ml kalio chlorido tirpalo, kuriame ištirpinta 0,1 mol
tirpinio. Raskite koncentraciją.
Atsakymas
3. Gėlėms
tręšti ištirpinta 0,3 mol natrio salietros. Tirpalo pagaminta
0,5
l. Raskite molinę koncentraciją.
Atsakymas
4. Kiek
molių natrio šarmo yra 450 ml tirpalo, kurio koncentracija 0,15
mol/l?
Atsakymas
5. Raskite
acto rūgšties molių skaičių, 750 ml tirpalo,
kurio koncentracija 0,4 mol/l.
Atsakymas
6. Kiek
molių sieros rūgšties ištirpę 1,5
l tirpalo, kurio
koncentracija 0,35 mol/l?
Atsakymas
7. Kokį
tūrį tirpalo galima pagaminti 1,5 mol/l koncentracijos azoto rūgšties
tirpalo, turint šios medžiagos 0,25 mol?
Atsakymas
8. Kiek
litrų sūrimo pagaminta, kurio koncentracija 0,25 mol/l iš
2 mol
natrio chlorido?
Atsakymas
9. Turime
4,5 mol karbamido, kiek tirpalo pagaminsime, kurio koncentracija 0,7 mol/l?
Atsakymas
10. Kiek
gramų natrio šarmo (NaOH) yra 4
l tirpalo, kurio koncentracija
0,04 mol/l?
Atsakymas
11. Raskite
vario sulfato (CuSO4) masę 2,5
l tirpalo, kurio
koncentracija 0,18 mol/l.
Atsakymas
12. Kokia
masė kalcio chlorido (CaCl2) yra 3
l tirpalo, kurio
koncentracija 0,12 mol/l?
Atsakymas
13. Tirpinant
100 g gliukozės C6H12O6 pagaminta
500 ml
tirpalo. Kokia molinė koncentracija?
Atsakymas
14. 1,75
l tirpalo ištirpinta 8 g kalio šarmo (KOH). Kokia molinė
koncentracija?
Atsakymas
15. 5
l tirpalo yra 117 g valgomosios druskos (NaCl). Kokia tirpalo molinė
koncentracija?
Atsakymas
16.
Kokio tūrio vandens H2O litrais (l) ir kokios masės (g) kalio sulfato K2SO4 reiks, 1,5
l
0,1mol/l koncentracijos tirpalui paruošti?
Atsakymas

|
 Uždaviniai savarankiškam darbui
Uždaviniai savarankiškam darbui