|
 Teorija Teorija
Molis – medžiagos kiekio vienetas,
kuriame yra tiek atomų, molekulių, jonų, kiek 12 g anglies 12C
izotopo. Jis žymimas raide n. Tai SI sistemos
vienetas.
Žinant medžiagos sudėtį
masės dalimis arba procentais galima nustatyti jos formulę. Masės
dalį pavertę į gramus, galime naudoti molio skaičiavimo
formulę.
 Formulės
Formulės
n = m : M
n – molis (mol)
m – medžiagos
masė (g)
Sprendžiant
šiuos uždavinius, m atitiks elemento masės dalį
junginyje.
M – elemento
molio masė (g/mol)
 Uždavinių sprendimo pavyzdžiai Uždavinių sprendimo pavyzdžiai
Uždavinys
1
|
Nežinomą junginį sudaro
46,6 % azoto ir 53,4 % deguonies. Junginio santykinė molekulinė masė
30. Raskite junginio formulę.
|
| Duota: w(N) =
m(N) 46,6 %
= 46,6g
w(O) = m(O) 53,4 % = 53,4g
M(N) = 14 g/mol
M(O) = 16 g/mol
Rasti:
junginio formulę
Formulė:
n = m : M
Sprendimas:
-
Randame
azoto molių skaičių:
n(N) = 46,6 g : 14 g/mol = 3,33 mol
-
Randame
deguonies molių skaičių:
n(O) = 53,4 g : 16 g/mol = 3,33 mol
-
Gautus
molius paverčiame sveikais skaičiais (dalindami iš mažiausio),
šiuo
atveju abu skaičiai vienodi.
n(N) : n(O) = (3,33 : 3,33) : (3,33
: 3,33) = 1 : 1
Gavome formulę, kurioje 1 azoto ir 1 deguonies atomai NO
-
Skaičiuojame
santykinę molekulinę masę (patikrinimui):
Mr(NO) = 14 + 16 = 30
Atsakymas: NO.
|
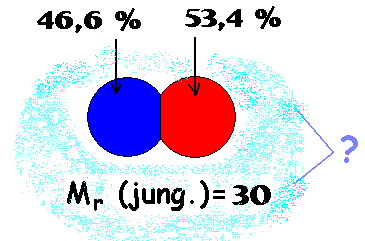
|
Uždavinys
2
|
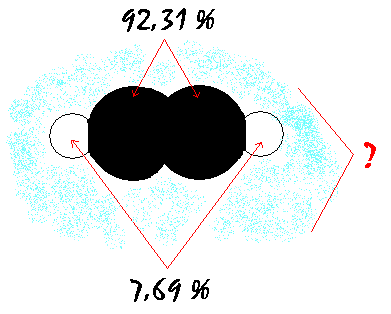
Junginys sudarytas iš
92,31 % anglies
ir 7,69 % vandenilio. Šio junginio tankis vandenilio atžvilgiu 13.
Raskite junginio formulę.
|
| Duota:
w(C) = m(C) 92,31 % = 92,34 g
w(H) = m(H) 7,69 % = 7,69 g
M(C) = 12 g/mol
M(H) = 1 g/mol
Rasti: junginio formulę
Formulės: n =
m : M
M(j) = DH2 x MH2
Sprendimas:
-
Randame
C molių skaičių:
n(C) = 92,31 g : 12 g/mol = 7,69 mol
-
Randame
H molių skaičių:
n(H) = 7,69 g : 1 g/mol = 7,69 mol
-
Dalijame
iš mažiausio molių skaičiaus:
n(C) : n(H) = (7,69 mol : 7,69 mol) : (7,69 mol : 7,69 mol)
Rasta 1 mol C ir 1 mol H
-
Randame
CH molinę masę:
M(CH) = 12 + 1 = 13 g/mol
-
Randame
junginio molinę masę:
M(j.) = 13 x 2 = 26 g/mol
-
Randame
kiek kartų reiks dauginti anglies ir vandenilio molių skaičių:
K = masė pagal vandenilį : masė gauto junginio
K = 2
-
Dauginame
anglies ir vandenilio molių skaičių iš 2.
gauta formulė C2H2
-
Skaičiuojame
C2H2 molinę masę:
M(C2H2) = 12 x 2 + 1 x 2 = 26 g/mol
Atsakymas: C2H 2.
|
|
 Uždaviniai savarankiškam darbui Uždaviniai savarankiškam darbui
1. Nežinomas
junginys sudarytas iš 42, 86 % anglies ir iš 57,14 % deguonies.
Junginio molinė masė 28 g/mol. Raskite junginio formulę.
Atsakymas
2.
Eksperimentiškai nustatyta, kad junginys sudarytas iš 11,11 % vandenilio ir
88,89 % deguonies. Jo molinė masė 18 g/mol. Raskite
junginio
formulę.
Atsakymas
3. Nustatyta
junginio procentinė sudėtis. Jį sudaro 70 % geležies ir
30 % deguonies, molinė masė - 160 g/mol. Raskite junginio formulę.
Atsakymas
4. Junginys
sudarytas iš natrio, deguonies ir vandenilio. Žinoma, kad jame
yra: 57,5 % natrio, 40 % deguonies ir 2,5 % vandenilio. Nustatykite junginio
formulę.
Atsakymas
5. Nustatyta,
jog junginys sudarytas iš 2,04 % vandenilio, 32,65 % sieros ir 65,31 %
deguonies. Šio junginio molinė masė 98 g/mol. Raskite junginio
formulę.
Atsakymas
6.
Dujinis junginys sudarytas iš 42,86 % anglies ir 57,14 % deguonies. Šio
junginio tankis vandenilio atžvilgiu 14. Raskite
junginio
formulę.
Atsakymas
7.
Junginys sudarytas iš 27,27 % angliesir 72,73 % deguonies. Šio junginio
tankis azoto atžvilgiu 1,571. Raskite
junginio
formulę.
Atsakymas
8.
Dujinė medžiaga sudaryta iš 30,43 % azoto ir 69,57 % deguonies. Tankis
anglies monoksido atžvilgiu 1,643. Raskite
junginio
formulę.
Atsakymas
9.
Junginys sudarytas iš 82,35 % azoto ir 17,65 % vandenilio. Tankis vandenilio
atžvilgiu 8,5. Raskite
junginio
formulę.
Atsakymas
10.
Junginys sudarytas iš 75 % anglies ir 25 % vandenilio. Tankis vandenilio
atžvilgiu 8. Raskite
junginio
formulę.
Atsakymas
11.
Dailininkai vitražų kūrimui naudoja spalvotą stiklą.
Raskite mėlynojo stiklo, kurį sudaro: 31,47 % natrio oksido Na2O,
38,07 % kobalto oksido CoO, 30,46 % silicio oksido SiO2 formulę.
Atsakymas
12.
Langų gamybai naudojamame stikle yra 12,97 % natrio
oksido (Na2O), 11,72 % kalcio oksido (CaO) ir 75,31 % silicio
oksido (SiO2). Nustatykite stiklo formulę.
Atsakymas

|